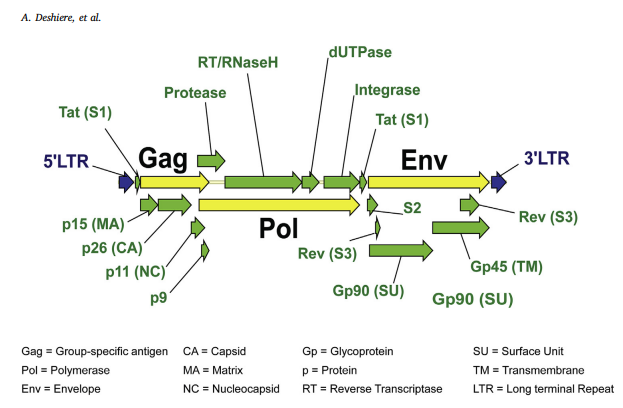
« Caractérisation des interactions virus-cellule hôte du virus de l’anémie infectieuse équine et exploration de nouvelles approches thérapeutiques »


Cécile SCHIMMICH a effectué ses travaux de recherche au sein de l’unité PhEED du laboratoire de Santé animale de l’Anses, hébergée dans les locaux de Normandie Équine Vallée à Goustranville.
Cécile SCHIMMICH a poursuivi un triple objectif :
Ses travaux de recherche visaient à caractériser les interactions cellule-hôte du virus de l’anémie infectieuse équine, à explorer de nouvelles approches thérapeutiques pour combattre cette maladie et à développer des médicaments antiviraux pour combattre cette maladie qui n’a aujourd’hui aucun traitement associé.
Pourquoi étudier cette maladie ?
L’anémie infectieuse équine (AIE) n’est pas une maladie contagieuse au sens strict : elle se transmet entre équidés par du sang contaminé uniquement, via l’intermédiaire de piqûres d’insectes (en particulier les taons) ou l’intermédiaire de matériel contaminé (utilisation d’une même aiguille contaminée pour prélever plusieurs chevaux par exemple). Le virus n’est pas transmissible à l’homme.
Un cheval contaminé reste porteur du virus dans le sang tout au long de sa vie, et peut ainsi contribuer à la contamination de ses congénères. L’anémie infectieuse est une maladie grave, qui peut entrainer la mort de l’équidé. Il n’existe aucun traitement, ni aucun vaccin.
Que savions-nous ?
Le virus de l’anémie infectieuse équine (VAIE) est un lentivirus équin apparenté au virus de l’immunodéficience humaine de type 1 (VIH-1). Les deux virus sont apparentés au sein de la famille des Retroviridae, mais leurs manifestations cliniques sont différentes car le VAIE provoque une infection persistante de longue durée sans dysfonctionnement immunitaire progressif dans la plupart des cas.
Aujourd’hui, aucun traitement n’est approuvé contre le VAIE, contrairement au VIH-1, gérable par une thérapie antirétrovirale, connue sous le nom de HAART (traitement antirétroviral hautement actif) ou cART (traitement antirétroviral combiné).
De plus, aucune information sur l’efficacité des médicaments antirétroviraux contre le VAIE n’est disponible dans la littérature.
Comment observer le virus ?
A. Photo au microscope optique de cellules de derme équin infectées :
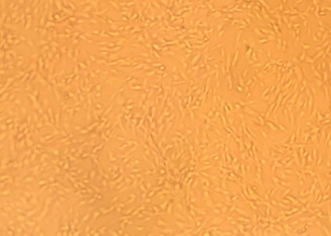
Source : Cécile SCHIMMICH, 2022, ANSES, Laboratoire de santé animale, Unité PhEED
Au grossissement x400 d’un microscope optique, nous observons des cellules du derme équin : des fibroblastes. Le virus de l’anémie infectieuse équine infecte ces cellules in vitro. Nous pouvons vérifier cette infection grâce à des méthodes de détection moléculaire (PCR), mais aucun changement visuel ne peut témoigner de cette infection au microscope optique.
B. Photo en microscopie à fluorescence de cellules de derme équin infectées :
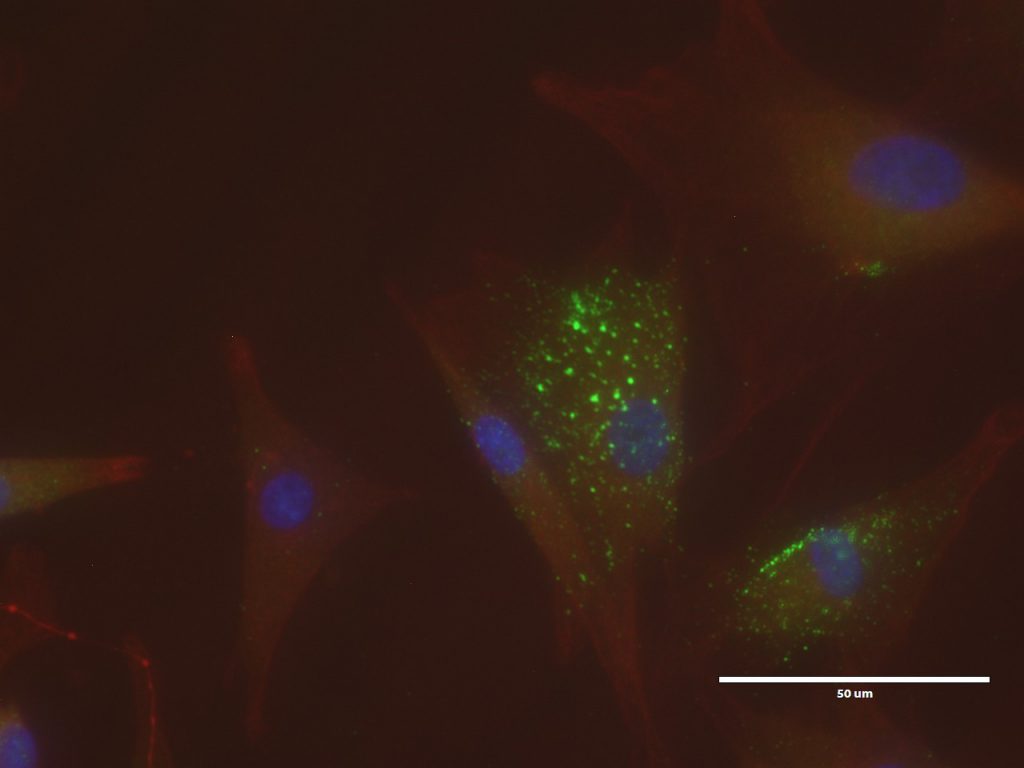
Source : Delphine GAUDAIRE, 2017, ANSES, Laboratoire de santé animale, Unité PhEED
La technique d’Immuno-Fluorescence permet d’observer la présence de particules virales dans des cellules infectées à l’aide de la microscopie : dans une cellule du derme équin infectée, le virus est marqué en vert grâce à un anticorps couplé à la GFP, protéine fluorescente verte, le noyau de la cellule en bleu par le marquage DAPI et la tubuline en rouge par le marquage d’une protéine structurale de la cellule.
Comment se propagent les particules virales ?
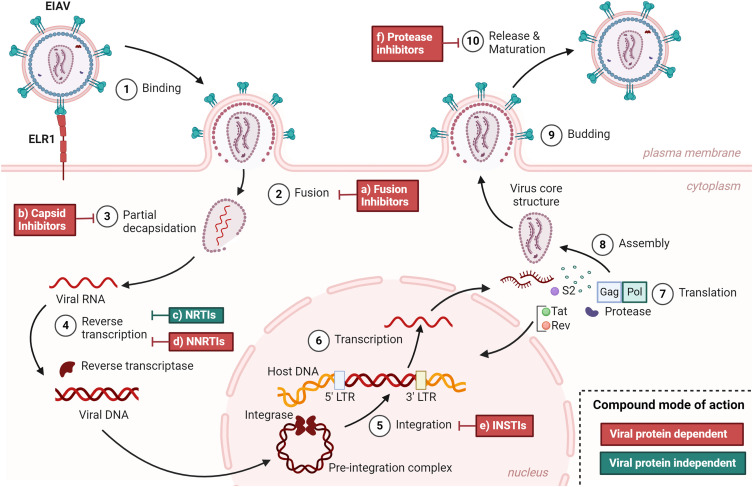
Le VAIE est un rétrovirus : il va infecter les cellules de l’hôte, convertir son génome ARN simple brin (grâce à la transcriptase inverse) en un ADN double brin, qui va être intégré au génome de la cellule hôte. À partir de ce mécanisme complexe, des particules virales vont pouvoir être produites et relarguées en dehors de la cellule pour infecter d’autres cellules.
Qu’avons-nous appris ?
Aucune information n’étant disponible sur l’efficacité des médicaments antirétroviraux contre le VAIE, une étude a donc été menée afin d’évaluer l’effet antiviral in vitro de 18 composés antirétroviraux approuvés par la Food and Drug Administration (FDA), dans un modèle d’infection in vitro de cellules équines avec une souche de référence du VAIE.
Des cellules dermiques équines, ainsi que des cellules mononucléaires du sang périphérique équin ont été traitées avec des concentrations de médicaments non cytotoxiques et infectées par le VAIE. La libération relative de virus dans les surnageants de culture a été évaluée par quantification relative de l’ARN viral via RTqPCR et l’ADN viral comprenant l’intégration provirale dans le génome cellulaire a été évalué par qPCR des cellules infectées, toutes deux après extraction d’acide nucléique. Sur les 18 médicaments testés, 13 ont montré un effet antiviral significatif contre le VAIE in vitro.
Commencé en novembre 2021, ces travaux de recherche ont notamment permis d’identifier 13 médicaments ayant un effet antiviral significatif contre le virus de l’VAIE in vitro. Ils s’agit donc d’une découverte très intéressante montrant les similitudes entre le VIH-1 et l’VAIE et ouvrant la possibilité de traiter l’anémie infectieuse équine pour éviter la propagation de la maladie.